Gujarat Board GSEB Solutions Class 10 Science Chapter 1 રાસાયણિક પ્રક્રિયાઓ અને સમીકરણો Textbook Questions and Answers, Intext Questions, Textbook Activites Pdf.
રાસાયણિક પ્રક્રિયાઓ અને સમીકરણો Class 10 GSEB Solutions Science Chapter 1
GSEB Class 10 Science રાસાયણિક પ્રક્રિયાઓ અને સમીકરણો Textbook Questions and Answers
સ્વાધ્યાયના પ્રશ્નોત્તર
પ્રશ્ન 1.
નીચે આપેલ પ્રક્રિયા માટેનાં વિધાનો પૈકી કયાં ખોટાં છે?
2PbO(s) + C(s) → 2Fb(s) + CO2(g)
(a) લેડ રિડક્શન પામે છે.
(b) કાર્બન ડાયોક્સાઇડ ઑક્સિડેશન પામે છે.
(c) કાર્બન ઑક્સિડેશન પામે છે.
(d) લેડ ઑક્સાઈડ રિડક્શન પામે છે.
(i) (a) અને (b)
(ii) (a) અને (c)
(iii) (a), (b) અને (C)
(iv) આપેલ તમામ
ઉત્તર:
(1) (a) અને (b)
પ્રશ્ન 2.
Fe2O3 + 2Al → Al2O3 + 2Fe
ઉપર દર્શાવેલી પ્રક્રિયા શેનું ઉદાહરણ છે?
(a) સંયોગીકરણ પ્રક્રિયા
(b) દ્વિવિસ્થાપન પ્રક્રિયા
(c) વિઘટન પ્રક્રિયા
(1) વિસ્થાપન પ્રક્રિયા
ઉત્તર:
(d) વિસ્થાપન પ્રક્રિયા
![]()
પ્રશ્ન 3.
આયર્નના ભૂકામાં મંદ હાઈડ્રોક્લોરિક ઍસિડ ઉમેરતાં શું થાય છે? સાચો ઉત્તર લખો.
(a) હાઇડ્રોજન વાયુ અને આયર્ન ફ્લોરાઇડ ઉદ્ભવે છે.
(b) ક્લોરિન વાયુ અને આયર્ન હાઇડ્રૉક્સાઈડ ઉદ્ભવે છે.
(c) કોઈ પ્રક્રિયા થતી નથી.
(d) આયર્ન ક્ષાર અને પાણી બને છે.
ઉત્તર:
(a) હાઇડ્રોજન વાયુ અને આયર્ન ક્લોરાઇડ ઉદ્ભવે છે.
પ્રશ્ન 4.
સમતોલિત રાસાયણિક સમીકરણ શું છે? રાસાયણિક સમીકરણોને શા માટે સમતોલિત કરવા જોઈએ?
ઉત્તર :
જે સમીકરણમાં પ્રક્રિયકો અને નીપજો બંને તરફ રહેલા પરમાણુઓની સંખ્યા સમાન હોય તેવા સમીકરણને સમતોલિત રાસાયણિક સમીકરણ કહે છે.
હવે દ્રવ્ય (દળ) સંરક્ષણ(સંચય)ના નિયમ મુજબ દ્રવ્યનું સર્જન કે વિનાશ થઈ શકતો નથી. આથી રાસાયણિક સમીકરણમાં રહેલા પ્રક્રિયકો અને નીપજોનું દળ સમાન રહેવું જોઈએ. દળ સમાન રાખવા સમીકરણમાં રહેલા પ્રત્યેક તત્ત્વના પરમાણુની સંખ્યા બંને બાજુ સમાન રહેવી જોઈએ. આથી રાસાયણિક સમીકરણને સમતોલિત કરવું આવશ્યક હોય છે.
પ્રશ્ન 5.
નીચેના વિધાનોને રાસાયણિક સમીકરણોમાં રૂપાંતરિત કરો અને ત્યારબાદ તેઓને સમતોલિત કરો:
(a) હાઇડ્રોજન વાયુ નાઇટ્રોજન વાયુ સાથે સંયોજાઈ એમોનિયા બનાવે છે.
(b) હાઇડ્રોજન સલ્ફાઈડ વાયુ હવામાં બળીને (દહન પામીને) સલ્ફર ડાયોક્સાઇડ અને પાણી આપે છે.
(c) બેરિયમ ક્લોરાઇડ એ ઍલ્યુમિનિયમ સલ્ફટ સાથે સંયોજાઈને ઍલ્યુમિનિયમ ક્લોરાઇડ આપે છે તેમજ બેરિયમ સલ્ફટના અવક્ષેપ આપે છે.
(d) પોટેશિયમ ધાતુ પાણી સાથે પ્રક્રિયા કરી પોટેશિયમ હાઇડ્રૉક્સાઈડ અને હાઈડ્રોજન વાયુ આપે છે.
ઉત્તર:

![]()
પ્રશ્ન 6.
નીચેનાં રાસાયણિક સમીકરણોને સમતોલિત કરોઃ
(a) HNO3 + Cu(OH)2 → Ca(NO3)2 + H2O
(b) NaOH + H2SO4 → Na2SO4 + H22O
(c) NaCl + AgNO3 → AgCl + NaNO3
(d) BaCl2 + H2SO4 → BaSO4 + HCl
ઉત્તર:
(a) 2HNO3 + Ca(OH)2 → Ca(NO3)2 + 2H2O
(b) 2NaOH + H2SO4 → Na2SO4 + 2H2O
(c) NaCl + AgNO3 → AgCl + NaNO3
(d) BaCl2 + H2SO4 → BaSO4 + 2HCl
પ્રશ્ન 7.
નીચે આપેલ રાસાયણિક પ્રક્રિયાઓ માટે સમતોલિત રાસાયણિક સમીકરણો લખો:
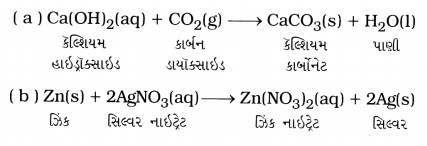
(a) કૅલ્શિયમ હાઇડ્રૉક્સાઇડ + કાર્બન ડાયોક્સાઈડ → કૅલ્શિયમ કાર્બોનેટ + પાણી
(b) ઝિંક + સિલ્વર નાઈટ્રેટ → ઝિંક નાઈટ્રેટ + સિલ્વર
(c) ઍલ્યુમિનિયમ + કૉપર ક્લોરાઇડ → ઍલ્યુમિનિયમ ક્લોરાઇડ + કૉપર
(d) બેરિયમ ક્લોરાઇડ + પોટેશિયમ સલ્ફટ → બેરિયમ સલ્ફટ + પોટેશિયમ ક્લોરાઈડ
ઉત્તર:

પ્રશ્ન 8.
નીચેના માટે સમતોલિત રાસાયણિક સમીકરણ લખો અને તે દરેક કિસ્સામાં પ્રક્રિયાનો પ્રકાર ઓળખો:
(a) પોટેશિયમ બ્રોમાઇડ(aq) + બેરિયમ આયોડાઈડ(aq) → પોટેશિયમ આયોડાઈડ(aq) + બેરિયમ બ્રોમાઈડ(aq)
(b) ઝિક કાર્બોનેટ(s) → ઝિંક ઑક્સાઈડ(s) + કાર્બન ડાયોક્સાઈડ(g)
(c) હાઇડ્રોજન(g) + ક્લોરિન(g) → હાઇડ્રોજન ક્લોરાઈડ(g)
(d) મૅગ્નેશિયમ(s) + હાઇડ્રોક્લોરિક ઍસિડ (aq) → મૅગ્નેશિયમ ક્લોરાઈડ(aq) + હાઈડ્રોજન(aq)
ઉત્તરઃ
(a) 2KBr(aq) + Bal(aq) → 2KI(aq) + BaBr2(s)
આપેલ પ્રક્રિયા એ દ્વિવિસ્થાપન પ્રક્રિયા છે.
(b ) ZnCO3(s) → ZnO(s) + CO2(g)
આપેલ પ્રક્રિયા એ વિઘટન પ્રક્રિયા છે.
(c) H2(g) + Cl2(g) + 2HCl(g)
આપેલ પ્રક્રિયા એ સંયોગીકરણ પ્રક્રિયા છે.
(d) Mg(s) + 2HCl(aq) → MgCl2(aq) + H2(g)
આપેલ પ્રક્રિયા એ વિસ્થાપન પ્રક્રિયા છે.
પ્રશ્ન 9.
ઉષ્માક્ષેપક અને ઉષ્માશોષક પ્રક્રિયા એટલે શું? ઉદાહરણો આપો.
ઉત્તર:
ઉષ્માક્ષેપક પ્રક્રિયા જે રાસાયણિક પ્રક્રિયામાં નીપજના નિર્માણની સાથે ઉષ્મા ઉત્પન્ન થતી હોય, તો તેવી પ્રક્રિયાને ઉષ્માક્ષેપક પ્રક્રિયા કહે છે.
દા. ત., કુદરતી વાયુ(CH4)ના દહનની પ્રક્રિયા એ ઉષ્માક્ષેપક પ્રક્રિયા છે.
CH4(g) + 2O2(g) → CO2(g) + 2H2O(g) + ઉષ્મા ઉષ્માશોષક પ્રક્રિયાઃ જે રાસાયણિક પ્રક્રિયામાં નીપજના નિર્માણ સાથે ઉષ્માનું શોષણ થતું હોય તેવી રાસાયણિક પ્રક્રિયાને ઉષ્માશોષક પ્રક્રિયા કહે છે.
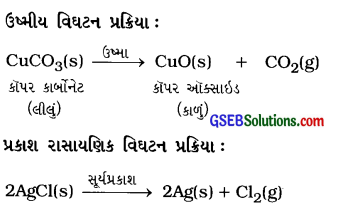
દા. ત., સિલ્વર ક્લોરાઈડનું સૂર્યપ્રકાશની હાજરીમાં વિઘટન થવું એ ઉષ્માશોષક પ્રક્રિયા છે.
![]()
![]()
પ્રશ્ન 10.
શ્વસનને ઉષ્માક્ષેપક પ્રક્રિયા શાથી ગણવામાં આવે છે? સમજાવો.
ઉત્તરઃ
પ્રશ્ન 11.
વિઘટન પ્રક્રિયાઓને સંયોગીકરણ પ્રક્રિયાઓની વિરુદ્ધ પ્રક્રિયા શા માટે કહેવાય છે? આ પ્રક્રિયાઓ માટેના સમીકરણો દર્શાવો.
ઉત્તર:
વિઘટન પ્રક્રિયામાં એકલ અણુને ઊર્જા આપતાં તે બે કે વધુ પરમાણુમાં વિયોજન (વિઘટન) પામે છે. જ્યારે સંયોગીકરણ પ્રક્રિયામાં વિઘટન પ્રક્રિયા કરતાં વિરુદ્ધ જોવા મળે છે. સંયોગીકરણ પ્રક્રિયામાં બે કે વધુ પરમાણુઓ ભેગા થઈને એકલ અણુ બને છે અને ઊર્જા મુક્ત થાય છે.
વિઘટન પ્રક્રિયાઓઃ
AB + ઊર્જા → A + B

સંયોગીકરણ પ્રક્રિયાઓઃ
A + B → AB + ઊર્જા
C(s) + O2(g) → CO2(g) + ઊર્જા
પ્રશ્ન 12.
એવી વિઘટન પ્રક્રિયાઓના એક-એક સમીકરણ દર્શાવો કે જેમાં ઊર્જા ઉષ્મા, પ્રકાશ અથવા વિદ્યુત સ્વરૂપે પૂરી પાડવામાં આવે છે.
ઉત્તર:
ઉષ્મા દ્વારા વિઘટન પ્રક્રિયા:

પ્રશ્ન 13.
વિસ્થાપન પ્રક્રિયા અને દ્વિવિસ્થાપન પ્રક્રિયા વચ્ચે શું તફાવત છે? આ પ્રક્રિયાઓ માટેનાં સમીકરણો લખો.
ઉત્તરઃ
વિસ્થાપન પ્રક્રિયામાં વધુ ક્રિયાશીલ તત્ત્વ એ ઓછા ક્રિયાશીલ તત્ત્વને તેના દ્રાવણમાંથી મુક્ત કરે છે.
જેમ કે, Zn અને Ag પૈકી Zn વધુ ક્રિયાશીલ હોવાથી તે ઓછા ક્રિયાશીલ Agને AgNO3ના દ્રાવણમાંથી મુક્ત કરે છે.
Zn(s) + 2AgNO3(aq) → Zn(NO3)2(aq) + 2Ag(s) જ્યારે દ્વિવિસ્થાપન પ્રક્રિયામાં બે પ્રક્રિયકો વચ્ચે આયનોની અદલા-બદલી અથવા આપ-લે થતી હોય છે. જેમ કે,
- Na2SO4(aq) + BaCl2(aq) → BaSO4(s) + 2NaCl(aq)
- 2KBr(aq) + BaI2(aq) → 2KI(aq) + BaBr2(s)
પ્રશ્ન 14.
સિલ્વરના શુદ્ધીકરણમાં કોપર ધાતુ દ્વારા સિલ્વર નાઈટ્રેટના દ્રાવણમાંથી ચાંદીની પ્રાપ્તિ વિસ્થાપન પ્રક્રિયા મારફતે થાય છે. તેમાં સમાવિષ્ટ પ્રક્રિયા લખો.
ઉત્તર:
Cu(s) + 2AgNO3(aq) → Cu(NO3)2(aq) + 2Ag(s)
![]()
પ્રશ્ન 15.
તમે અવક્ષેપન પ્રક્રિયાનો શું અર્થ કરો છો? ઉદાહરણ આપી સમજાવો.
ઉત્તર:
જે રાસાયણિક પ્રક્રિયા અદ્રાવ્ય અવક્ષેપ ઉત્પન્ન કરે છે. તેને અવક્ષેપન પ્રક્રિયા (Precipitation reaction) કહે છે. ઉદાહરણઃ
- AgNO3(aq) + NaCl(aq) → AgCl(s) (સફેદ અવક્ષેપ) + NaNO3(aq)
- BaCl2(aq) + K2SO4(aq) → BaSO4(s) (સફેદ અવક્ષેપ) + 2KCl(aq)
પ્રશ્ન 16.
ઑક્સિજનનું ઉમેરાવું અથવા દૂર થવું તેના આધારે નીચેનાં પદોને દરેકનાં બે ઉદાહરણ સહિત સમજાવોઃ
(1) ઑક્સિડેશન
(2) રિડક્શન
ઉત્તર:
(1) ઑક્સિડેશનઃ આ પ્રક્રિયામાં પદાર્થ (અણુ કે પરમાણુ) ઑક્સિજન મેળવે છે અથવા હાઈડ્રોજનને દૂર કરે છે. દા. ત.,
C + O2 → CO2
2Cu + O2 → 2Cu0
ઉપરની પ્રક્રિયાઓમાં ‘C’ અને ‘Cu’નું ઑક્સિડેશન થાય છે.
(2) રિડક્શનઃ આ પ્રક્રિયામાં પદાર્થ (અણુ કે પરમાણુ) ઑક્સિજન ગુમાવે છે અથવા હાઇડ્રોજન મેળવે છે.
દા. ત., CuO + H2 → Cu + H2O
CO2 + H → CO + H2O
ઉપરની પ્રક્રિયાઓમાં ‘cuO’ અને ‘COઝનું રિડક્શન થાય છે.
પ્રશ્ન 17.
એક ચળકતા કથ્થાઈ રંગના તત્ત્વ ને હવામાં ગરમ કરતાં તે કાળા રંગનું બને છે. તત્ત્વ ‘X’ તેમજ બનતા કાળા રંગના સંયોજનનું નામ આપો.
ઉત્તર:
અહીં, તત્ત્વ ‘X એ કોપર (Cu) છે. તેને હવામાં ગરમ કરતાં કાળા રંગનો કૉપર ઑક્સાઇડ (CuO) બને છે.
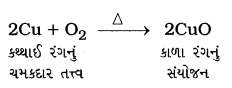
અહીં, Cuનું CuOમાં ઑક્સિડેશન થાય છે.
પ્રશ્ન 18.
લોખંડની વસ્તુઓ પર આપણે રંગ શા માટે લગાવીએ છીએ?
ઉત્તરઃ
ધાતુક્ષારણને લીધે લોખંડની વસ્તુ ઉપર કાટ લાગે છે. આથી કાટથી બચવા માટે લોખંડની સપાટી ઉપર રંગ લગાવવામાં આવે છે. જેને કારણે લોખંડ અને હવાનો સંપર્ક થતો નથી. પરિણામે લોખંડની વસ્તુ લાંબા સમય સુધી સુરક્ષિત રહે છે અને કાટ લાગતો નથી.
પ્રશ્ન 19.
તેલ તેમજ ચરબીયુક્ત ખાદ્ય પદાર્થોની સાથે નાઈટ્રોજન વાયુને ભરવામાં આવે છે. શા માટે?
ઉત્તર:
તેલ તેમજ ચરબીયુક્ત ખાદ્ય પદાર્થો હવામાંના ઑક્સિજન સાથે પ્રક્રિયા કરીને ખાદ્ય પદાર્થોને ખોરો કરે છે. આવા ખાદ્ય પદાર્થો સ્વાથ્ય માટે નુકસાનકારક છે. આથી ખોરાકને બગડતો અટકાવવા માટે તેમાં ઍન્ટિ-ઑક્સિડન્ટ તરીકે નાઈટ્રોજન જેવા નિષ્ક્રિય વાયુને ભરવામાં આવે છે.
પ્રશ્ન 20.
નીચેનાં પદોને તે દરેકના એક ઉદાહરણ સહિત સમજાવોઃ
(a) ક્ષારણ
(b) ખોરાપણું
ઉત્તર:
(a) ક્ષારણઃ
બધી જ ધાતુઓને હવામાં ખુલ્લી રાખતાં તેમાં ક્ષારણ જોવા મળે છે. ધાતુની ભેજ, ઍસિડ અને વાતાવરણના વાયુઓ સાથેની પ્રક્રિયાથી બનતાં સંયોજનોનું ધાતુની સપાટી પર પડ બને છે, જેને ક્ષારણ કહે છે.
કાટ લાગવો એ એવી પ્રક્રિયા છે કે જેમાં લોખંડ ધાતુ, હવા અને ભેજ સાથે પ્રક્રિયા કરીને લાલાશપડતો કથ્થાઈ રંગનો પાઉડર બનાવે છે, જેને કાટ લાગવો કહે છે. આમ, ક્ષારણને લીધે ધાતુની ચમક ઘટે છે.
![]()
(b) ખોરાપણું :
પાણીમાં હાઈડ્રોજન અને ઑક્સિજન H: O)નો ગુણોત્તર 2: 1 છે. પ્રવૃત્તિ દ્વારા સાબિત કરો.
ઉત્તર:
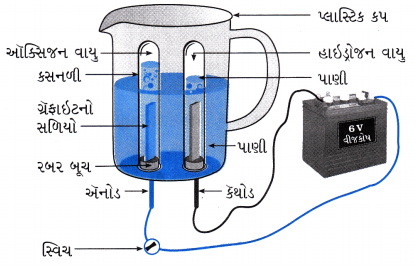
એક પ્લાસ્ટિકનો પહોળો કપ લો. તેના તળિયે બે કાણાં પાડી રબરના બૂચ ભરાવી દો. રબરના બૂચમાંથી કાર્બન(ગ્રેફાઇટ)ના ધ્રુવો આકૃતિમાં દર્શાવ્યા પ્રમાણે પસાર કરો.
- 6vની બૅટરી સાથે વિદ્યુતધ્રુવોને જોડો.
- કપમાં પાણી એટલું ભરો કે જેથી વિદ્યુતધ્રુવો ડૂબે. પછી તેમાં મંદ સક્યુરિક ઍસિડનાં થોડાંક ટીપાં નાખો.
- હવે, આકૃતિમાં દર્શાવ્યા મુજબ બંને વિદ્યુતધ્રુવો પર કસનળી ઊંધી મૂકો.
- વિદ્યુતપ્રવાહ ચાલુ કરી, થોડોક સમય માટે ઉપરોક્ત સાધનને જેમ છે તેમ રહેવા દો.
- તમે જોશો કે બંને વિદ્યુતધ્રુવો પર પરપોટા ઉભવશે, જે દર્શાવે છે કે પાણીનું વિદ્યુતવિભાજન થાય છે.
- કૅથોડ પરની કસનળીમાં એકત્રિત થતા હાઈડ્રોજન વાયુનું કદ એ ઍનોડ પરની કસનળીમાં એકત્રિત થતા ઑક્સિજન વાયુ કરતાં બમણું હોય છે.
- એક વાર કસનળી વાયુથી સંપૂર્ણ ભરાઈ જાય ત્યારે સાવચેતીથી તેને દૂર કરો.
- સળગતી દિવાસળી અથવા મીણબત્તી જ્યારે કૅથોડ પર એકત્રિત થયેલ વાયુની કસનળી પાસે લાવતાં ધડાકાભેર સળગી ઊઠે છે, જે હાઇડ્રોજન વાયુની હાજરી સૂચવે છે.
GSEB Class 10 Science રાસાયણિક પ્રક્રિયાઓ અને સમીકરણો Intext Questions and Answers
Intext પ્રજ્ઞોત્તર (પા.પુ. પાના નં. 6)
પ્રશ્ન 1.
મૅગ્નેશિયમની પટ્ટીને હવામાં સળગાવતા પહેલાં શા માટે સાફ કરવામાં આવે છે?
ઉત્તર:
મૅગ્નેશિયમ ધાતુ ખૂબ જ ક્રિયાશીલ હોવાથી તેને હવામાં ખુલ્લી રાખતાં તેની બહારની સપાટી પર MgOનું નિષ્ક્રિય પડ બને છે.
Mg + O2 → MgO
આ MOના નિષ્ક્રિય પડને કાચપેપર વડે સાફ કરવાથી મૅગ્નેશિયમની પટ્ટી સરળતાથી ઑક્સિજન સાથે પ્રક્રિયા કરે છે. આથી મૅગ્નેશિયમની પટ્ટીને હવામાં સળગાવતા પહેલાં સાફ કરવામાં આવે છે.
પ્રશ્ન 2.
નીચે દર્શાવેલ રાસાયણિક પ્રક્રિયાઓ માટે સમતોલિત સમીકરણ લખો :
(1) હાઇડ્રોજન + ક્લોરિન → હાઇડ્રોજન ક્લોરાઇડ
(2) બેરિયમ ક્લોરાઇડ + ઍલ્યુમિનિયમ સલ્ફટ → બેરિયમ સલ્ફટ + ઍલ્યુમિનિયમ ક્લોરાઇડ
(3) સોડિયમ + પાણી → સોડિયમ હાઇડ્રૉક્સાઇડ + હાઇડ્રોજન
ઉત્તર:
(1) H2 + Cl2 → 2Hcl
(2) 3BaCl2 + Al2(SO4)O3 → 3BaSO4 + 2AlCl3
(3) 2Na + 2H2O → 2NaOH + H2
પ્રશ્ન 3.
નીચે દર્શાવેલ પ્રક્રિયાઓ માટે ભૌતિક અવસ્થાઓની સંજ્ઞા સહિતના સમતોલિત રાસાયણિક સમીકરણ લખો :
(1) બેરિયમ ક્લોરાઇડ અને સોડિયમ સલ્ફટનાં પાણીમાં બનાવેલા દ્રાવણો વચ્ચે પ્રક્રિયા થઈ અદ્રાવ્ય બેરિયમ સલ્ફટ અને સોડિયમ ક્લોરાઇડનું દ્રાવણ મળે છે.
(2) સોડિયમ હાઇડ્રૉક્સાઇડ દ્રાવણ (પાણીમાં) હાઇડ્રોક્લોરિક ઍસિડના દ્રાવણ (પાણીમાં) સાથે પ્રક્રિયા કરી સોડિયમ ક્લોરાઇડ દ્રાવણ અને પાણી ઉત્પન્ન કરે છે.
ઉત્તર:

Intext પ્રશ્નોત્તર (પા.પુ. પાના નં. 10)
પ્રશ્ન 1.
પદાર્થ ‘x’નું દ્રાવણ ધોળવા (White washing) માટે વપરાય છે.
(1) પદાર્થ ‘x’નું નામ આપો અને તેનું સૂત્ર લખો.
(2) પદાર્થ ‘x’ની પાણી સાથેની પ્રક્રિયા લખો.
ઉત્તર:
(1) પદાર્થ ‘X’ એ કૅલ્શિયમ ઑક્સાઈડ છે. જેનું સૂત્ર CaO છે.
(2) કૅલ્શિયમ ઑક્સાઇડ પાણી સાથે તીવ્રતાથી પ્રક્રિયા કરી ચૂનાનું નીતર્યું પાણી [Ca(OH)2] બનાવે છે અને અધિક પ્રમાણમાં ઉષ્મા મુક્ત કરે છે.
CaO + H2O → Ca(OH)2 + ઉષ્મા
![]()
પ્રશ્ન 2.
પ્રવૃત્તિ 1.7માં એક કસનળીમાં એકત્ર થતો વાયુનો જથ્થો એ બીજી કસનળીમાં એકત્ર થતા વાયુના જથ્થા કરતાં બમણો શા માટે છે? આ વાયુનું નામ દર્શાવો.
ઉત્તર:
પાણીના વિદ્યુતવિભાજન દરમિયાન હાઇડ્રોજન અને ઑક્સિજન અલગ મળે છે. પાણીમાં બે ભાગ હાઇડ્રોજન અને એક ભાગ ઑક્સિજન હોવાથી એક કસનળીમાં બે ભાગ હાઇડ્રોજન અને બીજી કસનળીમાં એક ભાગ ઑક્સિજન વાયુ મળે છે.
આમ, મળતા હાઇડ્રોજન અને ઑક્સિજન વાયુનું કદથી પ્રમાણ 2 : 1 છે.
![]()
(નોંધ : જુઓ આકૃતિ 1.6)
Intext પ્રશ્નોત્તર (પા.પુ. પાના નં. 13)
પ્રશ્ન 1.
જ્યારે કૉપર સલ્ફટના દ્રાવણમાં આયર્નની ખીલી ડુબાડવામાં આવે ત્યારે કૉપર સલ્ફટના દ્રાવણનો રંગ શા માટે બદલાય છે?
ઉત્તર:
આયર્નની ખીલીને કૉપર સલ્ફટના દ્રાવણમાં ડુબાડતાં, કૉપર કરતાં આયર્ન વધુ ક્રિયાશીલ હોવાથી તે કૉપરનું વિસ્થાપન કરે છે અને પરિણામે આયર્ન સલ્ફટ બને છે, જે લીલા રંગનો હોવાથી દ્રાવણનો રંગ બદલાય છે.

પ્રશ્ન 2.
પ્રવૃત્તિ 1.10માં દર્શાવ્યા સિવાયની કોઈ ઢિવિસ્થાપન પ્રક્રિયાનું ઉદાહરણ આપો.
ઉત્તર:
સોડિયમ કાર્બોનેટની કૅલ્શિયમ ક્લોરાઇડ સાથેની પ્રક્રિયાથી કૅલ્શિયમ કાર્બોનેટના અવક્ષેપ અને સોડિયમ ક્લોરાઈડ બને છે. આ પ્રક્રિયામાં કાર્બોનેટ અને ક્લોરાઇડ આયનનું આદાન-પ્રદાન થવાથી બે નવાં સંયોજનો બને છે.

આ પ્રક્રિયા દ્વિવિસ્થાપન પ્રક્રિયા છે.
પ્રશ્ન 3.
નીચે દર્શાવેલ પ્રક્રિયાઓમાં ઑક્સિડેશન પામતા અને રિડક્શન પામતા પદાર્થોને ઓળખો:
(1) 4Na(s) + O2(g) → 2Na2O(s)
(2) cuO(s) + H2(g) → Cu(s) + H2O(l)
ઉત્તરઃ
(1) 4Na(s) + O2(g) → 2Na2O(S)
આપેલ પ્રક્રિયામાં સોડિયમ (Na) ધાતુનું Na90માં ઑક્સિડેશન થાય છે, જ્યારે O2નું રિડક્શન થાય છે.
આમ, ઑક્સિડેશન પામતો પદાર્થ : Na2O
રિડક્શન પામતો પદાર્થ : O2
(2) CuO(s) + H2(g) → Cu(s) + H2O(l)
આપેલ પ્રક્રિયામાં CuO નું Cuમાં રિડક્શન થાય છે, જ્યારે H2નું H2O માં ઑક્સિડેશન થાય છે.
આમ, ઑક્સિડેશન પામતો પદાર્થ : H2O
રિડક્શન પામતો પદાર્થ : Cu
GSEB Class 10 Science રાસાયણિક પ્રક્રિયાઓ અને સમીકરણો Textbook Activities
પ્રવૃત્તિ 1.1 (પા.પુ. પાના નં. 1)
હેતુઃ મૅગ્નેશિયમની પટ્ટીનું હવામાં દહન કરવું.
સાવધાની: આ પ્રવૃત્તિ શિક્ષકની હાજરીમાં થાય તે જરૂરી છે. સુરક્ષા માટે શિક્ષક તેમજ વિદ્યાર્થી ચશ્માં પહેરે તે યોગ્ય છે.
પ્રવૃત્તિઃ

- લગભગ 2 cm લાંબી કાચપેપરથી ઘસેલી શુદ્ધ મૅગ્નેશિયમની પટ્ટી લો.
- તેને ચીપિયાથી પકડીને સ્પિરિટ લૅમ્પ કે બર્નરની જ્યોતમાં ગરમ કરો. આથી બનતી રાખ આકૃતિ 1.1માં દર્શાવ્યા મુજબ વૉચગ્લાસમાં એકઠી કરો.
- વૉચગ્લાસમાં એકઠી થતી રાખ એ મૅગ્નેશિયમ ઑક્સાઇડ છે.
સૂચનાઃ મૅગ્નેશિયમની પટ્ટીના દહન દરમિયાન શક્ય હોય ત્યાં સુધી આપણી આંખોને દૂર રાખો.
ઉપરોક્ત પ્રવૃત્તિ પરથી તમે શું અવલોકન કર્યું, તેના સંદર્ભમાં નીચેના પ્રશ્નોના ઉત્તર આપો:
પ્રશ્ન 1.
મૅગ્નેશિયમની પટ્ટી જ શા માટે લેવામાં આવે છે?
ઉત્તર:
મૅગ્નેશિયમની પટ્ટી ખૂબ જ ક્રિયાશીલ હોવાથી તેનું હવામાં સરળતાથી દહન થાય છે.
પ્રશ્ન 2.
મૅગ્નેશિયમની પટ્ટી શરૂઆતમાં કેવા રંગની હોય છે?
ઉત્તર:
મૅગ્નેશિયમની પટ્ટી શરૂઆતમાં કાચપેપરથી ઘસેલી હોવાથી ચમકતી શ્વેત રંગની હોય છે.
પ્રશ્ન 3.
મૅગ્નેશિયમની પટ્ટી બર્નરની જ્યોતમાં કેવી જ્યોતથી સળગે છે?
ઉત્તર:
મૅગ્નેશિયમની પટ્ટી બર્નરની જ્યોતમાં ઝગારા મારતી (પ્રજ્વલિત) સફેદ જ્યોતથી સળગે છે.
![]()
પ્રશ્ન 4.
વૉચગ્લાસમાં એકઠી થતી રાખ શેની હોય છે?
ઉત્તર:
વૉચગ્લાસમાં એકઠી થતી સફેદ રાખ મૅગ્નેશિયમ ઑક્સાઇડ (MgO)ની હોય છે.
(નોંધ : હવામાં O2 અને N2 હોવાથી મુખ્યત્વે Mg3O2 બને.તદ્ઘપરાંત અલ્પ પ્રમાણમાં Mg3N2 પણ બને.)
પ્રશ્ન 5.
મૅગ્નેશિયમ ઑક્સાઇડ બનવાની રાસાયણિક પ્રક્રિયા લખો.
ઉત્તર:
2Mg(s) + O2(g) ![]() 2MgO(s)
2MgO(s)
પ્રવૃત્તિ 1.2 (પા.પુ. પાના નં. 2)
હેતુ લેડ નાઇટ્રેટ અને પોટૅશિયમ આયોડાઇડ વચ્ચે થતી પ્રક્રિયા સમજવી.
પ્રવૃત્તિ
- એક સ્વચ્છ કસનળી લો.
- તેમાં લેડ નાઈટ્રેટનું દ્રાવણ લો.
- તેમાં પોટેશિયમ આયોડાઇડનું દ્રાવણ ઉમેરો.
ઉપરોક્ત પ્રવૃત્તિ પરથી તમે શું અવલોકન કર્યું, તેના સંદર્ભમાં નીચેના પ્રશ્નોના ઉત્તર આપો:
પ્રશ્ન 1.
લેડ નાઇટ્રેટના પાઉડરનો રંગ કેવો હોય છે?
ઉત્તર:
લેડ નાઇટ્રેટનો પાઉડર સફેદ રંગનો હોય છે.
પ્રશ્ન 2.
પોટેશિયમ આયોડાઇડના જલીય દ્રાવણનો રંગ કેવો હોય છે?
ઉત્તર:
પોટેશિયમ આયોડાઇડનું જલીય દ્રાવણ રંગવિહીન હોય છે.
પ્રશ્ન 3.
લેડ નાઇટ્રેટ અને પોટેશિયમ આયોડાઇડ વચ્ચે થતી રાસાયણિક પ્રક્રિયાનું સમતુલિત સમીકરણ લખો.
ઉત્તર:
Pb(NO3)2 (s) + 2KI(aq) → PbI2 + 2KNO3(s)
પ્રશ્ન 4.
PbI2 નો રંગ જણાવો.
ઉત્તર:
PbI2 નો રંગ પીળો છે.
પ્રશ્ન 5.
આ પ્રક્રિયા કયા પ્રકારની છે?
ઉત્તર:
આ પ્રક્રિયા દ્વિવિસ્થાપન પ્રકારની છે.
પ્રવૃત્તિ 1.3 (પા.પુ. પાના નં. 22.)
હેતુઃ ઝિક ધાતુ અને મંદ સક્યુરિક ઍસિડ અથવા મંદ હાઇડ્રોક્લોરિક ઍસિડ વચ્ચે થતી પ્રક્રિયા સમજવી.
સાવધાની: ઍસિડનો ઉપયોગ સાવધાનીથી કરો.
પ્રવૃત્તિ
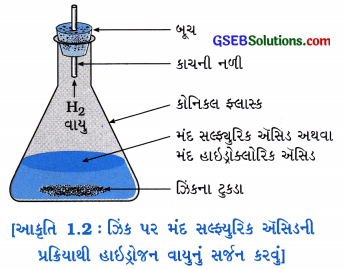
- એક કોનિકલ ફ્લાસ્ક લો.
- તેમાં ઝિક ધાતુના ટુકડા નાખો.
- પછી તેમાં મંદ સક્યુરિક ઍસિડ કે મંદ હાઇડ્રોક્લોરિક ઍસિડ છે ઉમેરો.
ઉપરોક્ત પ્રવૃત્તિ પરથી તમે શું અવલોકન કર્યું, તેના સંદર્ભમાં નીચેના પ્રશ્નોના ઉત્તર આપોઃ
પ્રશ્ન 1.
ઝિકના ટુકડાની આસપાસ શું દેખાય છે?
ઉત્તરઃ
ઝિકના ટુકડા, મંદ હાઇડ્રોક્લોરિક ઍસિડ સાથે પ્રક્રિયા કરી હાઇડ્રોજન વાયુ ઉત્પન્ન કરે છે. પરિણામે ઝિંકના ટુકડાની આસપાસ હાઇડ્રોજન વાયુના પરપોટા દેખાય છે.
![]()
પ્રશ્ન 2.
કોનિકલ ફ્લાસ્ક પર શી અસર થાય છે?
ઉત્તર:
કોનિકલ ફ્લાસ્ટ ગરમ થાય છે, જે સ્પર્શ કરીને અનુભવી શકાય છે.
પ્રશ્ન 3.
ઝિકના ટુકડા અને મંદ HCl વચ્ચે થતી પ્રક્રિયા લખો. ?
ઉત્તર:
Zn(s) + 2HCl(aq) → ZnCl2(aq) + H2(g)
પ્રશ્ન 4.
ઝિકના ટુકડા અને મંદ HCl વચ્ચે થતી પ્રક્રિયા કેવા પ્રકારની છે?
ઉત્તર:
ઝિકના ટુકડા અને મંદ HCl વચ્ચે થતી પ્રક્રિયા એ ઉષ્માક્ષેપક પ્રક્રિયા છે.
પ્રવૃત્તિ 1.4 (પા.પુ. પાના નં. 6)
હેતુઃ કૅલ્શિયમ ઑક્સાઈડ અને પાણી વચ્ચે થતી પ્રક્રિયા સમજવી.
પ્રવૃત્તિઃ
- એક બીકરમાં કેલ્શિયમ ઑક્સાઈડ (કળીચૂનો – CaO) લો.
- તેમાં ધીમે ધીમે પાણી ઉમેરો.
- આકૃતિ 1.3માં દર્શાવ્યા મુજબ બકરને હાથથી સ્પર્શ કરો.
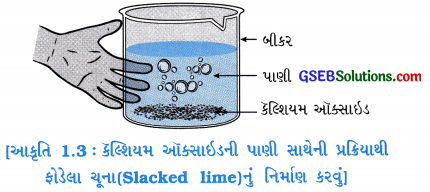
ઉપરોક્ત પ્રવૃત્તિ પરથી તમે શું અવલોકન કર્યું, તેના સંદર્ભમાં નીચેના પ્રશ્નોના ઉત્તર આપો :
પ્રશ્ન 1.
કળીચૂનો અને પાણી દ્વારા શું બને? પ્રક્રિયા લખો.
ઉત્તર:
કળીચૂનાની પાણી સાથેની પ્રક્રિયાથી Ca(OH), બને છે.
CaO(s) + H2O(l) → Ca(OH)2(aq)
પ્રશ્ન 2.
કળીચૂનાની પાણી સાથેની પ્રક્રિયાને શું કહે છે?
ઉત્તર:
કળીચૂનાની પાણી સાથેની પ્રક્રિયાને ચૂનાનું ફૂટવું (Slaking of lime) કહે છે.
પ્રશ્ન 3.
ઉપરોક્ત પ્રવૃત્તિમાં બકરને બહારથી સ્પર્શ કરતાં શું અનુભવો છો?
ઉત્તર:
બીકર ગરમ લાગે છે, કારણ કે પ્રક્રિયા દરમિયાન ઉષ્માં ઉત્પન્ન થાય છે.
![]()
પ્રશ્ન 4.
ફોડેલો ચૂનાનું રાસાયણિક સૂત્ર જણાવો.
ઉત્તર:
ફોડેલો ચૂનાનું રાસાયણિક સૂત્ર Ca(OH)2 છે.
પ્રવૃત્તિ 1.5 (પા.પુ. પાના નં. 80)
હેતુઃ ફેરસ સલ્ફટને ગરમ કરી વિઘટન પ્રક્રિયા સમજવી.
પ્રવૃત્તિઃ

- એક સૂકી ઉત્કલન નળી(જ્વલન નળી)માં આશરે 2 g સ્ફટિકમય ફેરસ સલ્ફટ લો.
- આ ઉત્કલન નળીને બર્નરની જ્યોત ઉપર ગરમ કરો.
- ગરમ કરતી વખતે સ્ફટિકમય ફેરસ સલ્ફટના રંગને ધ્યાનથી જુઓ.
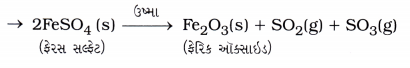
ઉપરોક્ત પ્રવૃત્તિ પરથી તમે શું અવલોકન કર્યું, તેના સંદર્ભમાં નીચેના પ્રશ્નોના ઉત્તર આપો?
પ્રશ્ન 1.
સ્ફટિકમય ફેરસ સલ્ફટનો રંગ કેવો છે?
ઉત્તર:
સ્ફટિકમય ફેરસ સલ્ફટનો રંગ લીલાશપડતો અથવા આછો લીલો છે.
પ્રશ્ન 2.
સ્ફટિકમય ફેરસ સલ્ફટને ગરમ કરતાં કયો રંગ બને છે? .
ઉત્તર:
સ્ફટિકમય ફેરસ સલ્ફટને ગરમ કરતાં Fe905 બનવાને કારણે લીલાશપડતા રંગમાંથી લાલાશપડતો કથ્થાઈ રંગ બને છે.
પ્રશ્ન 3.
સ્ફટિકમય ફેરસ સલ્ફટને ગરમ કરતાં નીકળતો વાયુ વિશિષ્ટ ગંધ ધરાવે છે. તેનું કારણ શું છે?
ઉત્તર:
સ્ફટિકમય ફેરસ સલ્ફટને ગરમ કરતાં વિશિષ્ટ વાસ ધરાવતો વાયુ ઉદ્ભવે છે. તેનું કારણ સલ્ફરનું દહન છે. સલ્ફરના દહનથી SO2 અને SO3 વાયુઓ ઉત્પન્ન થાય છે, જે તીવ્ર વાસ ધરાવે છે.
પ્રવૃત્તિ 1.6 (પા.પુ. પાના નં 8)
હેતુઃ લેડ નાઇટ્રેટના વિઘટનની પ્રક્રિયા સમજવી.
પ્રવૃત્તિ:
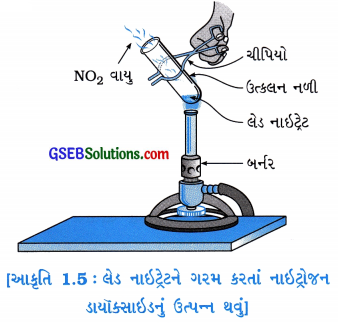
- એક કસનળીમાં આશરે 2 g લેડ નાઈટ્રેટનો પાઉડર લો.
- આકૃતિ 1.5માં દર્શાવ્યા મુજબ ચીપિયા વડે ઉત્કલન નળીને હોલ્ડર વડે પકડીને બર્નરની જ્યોત ઉપર ગરમ કરો.
- કોઈ ફેરફાર દેખાયો?
ઉપરોક્ત પ્રવૃત્તિ પરથી તમે શું અવલોકન કર્યું, તેના સંદર્ભમાં નીચેના પ્રશ્નોના ઉત્તર આપો?
પ્રશ્ન 1.
લેડ નાઇટ્રેટને ગરમ કરતાં ઉત્કલન નળીમાંથી કયા રંગનો વાયુ બહાર નીકળે છે?
ઉત્તર:
લેડ નાઇટ્રેટને ગરમ કરતાં ઉત્કલન નળીમાંથી કથ્થાઈ (બ્રાઉન) રંગનો NO2 વાયુ બહાર નીકળે છે.
![]()
પ્રશ્ન 2.
લેડ નાઇટ્રેટને ગરમ કરતાં થતી પ્રક્રિયા લખો.
ઉત્તર:

પ્રવૃત્તિ 1.7 (પા.પુ. પાના નં. 9)
હેતુઃ પાણીનું વિદ્યુતવિભાજન સમજવું.
પ્રવૃત્તિ:
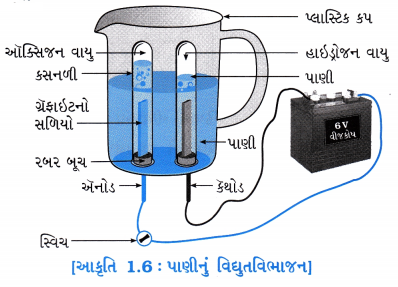
- આકૃતિ 1.6માં દર્શાવ્યા મુજબ એક પ્લાસ્ટિક કપના તળિયે બે છિદ્રો પાડી તેમાં રબરના બૂચ લગાવો.
- આકૃતિમાં દર્શાવ્યા મુજબ કાર્બન(ગ્રેફાઇટ)ના વિદ્યુતધ્રુવને પ્લાસ્ટિકના કપમાં મૂકી, તેની ઉપર કસનળીને ઊંધી ગોઠવો.
- કપમાં પાણી એટલું ઉમેરો કે જેથી વિદ્યુતધ્રુવો ડૂબેલા રહે.
- પાણીમાં મંદ સફ્યુરિક ઍસિડનાં થોડાં ટીપાં નાખો.
- વિદ્યુતધ્રુવોને 6vની બૅટરી સાથે જોડો.
- હવે વિદ્યુતપ્રવાહ શરૂ કરો. થોડીક વાર રાહ જુઓ.
ઉપરોક્ત પ્રવૃત્તિ પરથી તમે શું અવલોકન કર્યું, તેના સંદર્ભમાં નીચેના પ્રશ્નોના ઉત્તર આપો:
પ્રશ્ન 1.
વિદ્યુતધ્રુવ એટલે શું?
ઉત્તર:
વિદ્યુતવિભાજનના દ્રાવણમાં ડુબાડેલ પ્લેટિનમ કે કાર્બનના સળિયા કે જેની સપાટી ઉપર રાસાયણિક પ્રક્રિયાઓ થાય છે. તેને વિદ્યુતધ્રુવ કહે છે.
પ્રશ્ન 2.
પાણીના વિદ્યુતવિભાજન દરમિયાન ઍનોડ વિદ્યુતધ્રુવ ઉપર ક્યો વાયુ ઉત્પન્ન થાય છે?
ઉત્તર:
પાણીના વિદ્યુતવિભાજન દરમિયાન ઍનોડ વિદ્યુતધ્રુવ ઉપર ઑક્સિજન વાયુ ઉત્પન્ન થાય છે.
પ્રશ્ન 3.
પાણીના વિદ્યુતવિભાજન દરમિયાન કેથોડ વિદ્યુતધ્રુવ ઉપર કયો વાયુ ઉત્પન્ન થાય છે?
ઉત્તર:
પાણીના વિદ્યુતવિભાજન દરમિયાન કેથોડ વિદ્યુતધ્રુવ ઉપર હાઇડ્રોજન વાયુ ઉત્પન્ન થાય છે.
પ્રશ્ન 4.
પ્રયોગ દરમિયાન બંને કસનળીમાં ઉત્પન્ન થતા વાયુના કદ સમાન હોય છે?
ઉત્તર:
ના
![]()
પ્રશ્ન 5.
પાણીના વિદ્યુતવિભાજનની પ્રક્રિયા લખો.
ઉત્તર:
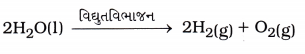
પ્રશ્ન 6.
ઉત્પન્ન થતાં O2(g) અને H2ને(g) સળગતી મીણબત્તી પાસે લઈ જતાં શું જોવા મળે છે?
ઉત્તર:
O2(g) સળગતો નથી, જ્યારે H2(g) સળગે છે.
પ્રવૃત્તિ 1.8 (પા.પુ. પાના નં. 9)
હેતુઃ સિલ્વર ક્લોરાઇડનું સૂર્યપ્રકાશની હાજરીમાં વિઘટન સમજવું.
પ્રવૃત્તિઃ

- એક બાષ્પવાટકી(ચાઇના ડિશ)માં આશરે 2 g સિલ્વર ક્લોરાઇડ લો.
- આ બાષ્પવાટકીને થોડાક સમય માટે સૂર્યપ્રકાશમાં મૂકો.
ઉપરોક્ત પ્રવૃત્તિ પરથી તમે શું અવલોકન કર્યું, તેના સંદર્ભમાં નીચેના પ્રશ્નોના ઉત્તર આપોઃ
પ્રશ્ન 1.
સૂર્યપ્રકાશમાં મૂકતાં પહેલાં સિલ્વર ક્લોરાઇડ કયા રંગનો હતો?
ઉત્તર:
સૂર્યપ્રકાશમાં મૂકતાં પહેલાં સિલ્વર ક્લોરાઇડ સફેદ રંગનો હતો.
પ્રશ્ન 2.
સૂર્યપ્રકાશમાં થોડો સમય રાખી મૂકતાં સિલ્વર ક્લોરાઇડના રંગમાં શું ફેરફાર થાય છે?
ઉત્તર:
સૂર્યપ્રકાશમાં થોડો સમય રાખી મૂકતાં સિલ્વર ક્લોરાઇડનો રંગ સફેદમાંથી ભૂખરો થાય છે.
પ્રશ્ન 3.
સૂર્યપ્રકાશની હાજરીમાં થતી બે વિઘટન પ્રક્રિયા લખો.
ઉત્તર:
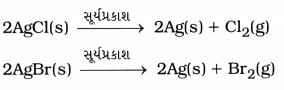
પ્રશ્ન 4.
શું સિલ્વર બ્રોમાઇડનું સૂર્યપ્રકાશની હાજરીમાં વિઘટન થાય ખરું?
ઉત્તર:
હા
પ્રશ્ન 5.
AgCl અને AgBrનો ઉપયોગ ક્યાં થાય છે?
ઉત્તર:
AgCl અને AgBrનો ઉપયોગ શ્યામ અને શ્વેત (Black and white) ફોટોગ્રાફીમાં થાય છે.
પ્રવૃત્તિ 1.9 (પા.પુ. પાના નં. 10)
હેતુ લોખંડની ખીલી અને કૉપર સલ્ફટના દ્રાવણ વચ્ચે થતી પ્રક્રિયા સમજવી.
પ્રવૃત્તિઃ
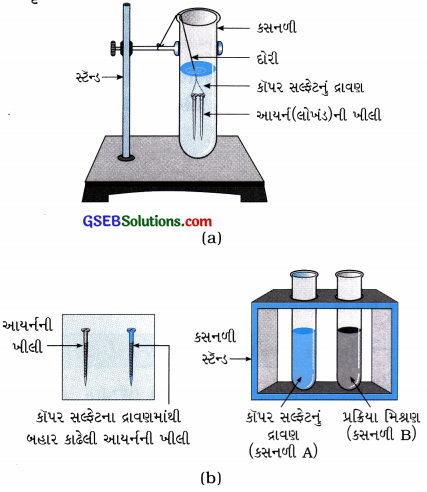
[આકૃતિ 1.8: (a) કૉપર સલ્ફટના દ્રાવણમાં ડુબાડેલી આયર્ન(લોખંડ)ની ખીલીઓ (b) પ્રયોગ પહેલાં તેમજ પ્રયોગ બાદ આયર્ન(લોખંડ)ની ખીલીઓ અને કૉપર સલ્ફટના દ્રાવણની સરખામણી]
- કાચપેપરથી સાફ કરેલી આયર્નની ત્રણ ખીલી લો.
- બે કસનળી પર A અને B લખો. પ્રત્યેક કસનળીમાં 10 mL કૉપર સલ્ફટનું દ્રાવણ લો.
- આકૃતિ 1.8 (a)માં દર્શાવ્યા મુજબ આયર્નની ખીલીને દોરીથી બાંધી 20 મિનિટ સુધી કૉપર સલ્ફટના દ્રાવણમાં ડુબાડી રાખો. તુલના કરવા માટે એક ખીલીને દ્રાવણથી અલગ રાખો.
- 20 મિનિટ પછી બંને ખીલીને દ્રાવણમાંથી બહાર કાઢો.
- બંને ખીલીના રંગની તુલના બહાર રાખેલ ખીલી સાથે કરો.
- કૉપર સલ્ફટના દ્રાવણના રંગની તીવ્રતાની સરખામણી કરો.
ઉપરોક્ત પ્રવૃત્તિ પરથી તમે શું અવલોકન કર્યું, તેના સંદર્ભમાં નીચેના પ્રશ્નોના ઉત્તર આપો :
પ્રશ્ન 1.
આયર્નની ખીલીને CuS0ના દ્રાવણમાં મૂકતાં તે કયા રંગની બને છે?
ઉત્તર:
આયર્નની ખીલી કથ્થાઈ રંગની બને છે.
પ્રશ્ન 2.
પ્રયોગ દરમિયાન કૉપર સલ્ફટના દ્રાવણનો ભૂરો રંગ કેવો બનશે?
ઉત્તર:
પ્રયોગ દરમિયાન કૉપર સલ્ફટના દ્રાવણનો ભૂરો રંગ આછો લીલો બનશે.
![]()
પ્રશ્ન 3.
આયર્નની ખીલીને કૉપર સલ્ફટના દ્રાવણમાં ડુબાડતાં કઈ પ્રક્રિયા થાય છે?
ઉત્તર:
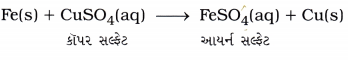
પ્રશ્ન 4.
આયર્નની ખીલીની કૉપર સલ્ફટ સાથેની પ્રક્રિયા કયા પ્રકારની છે?
ઉત્તર:
આયર્નની ખીલીની કૉપર સલ્ફટ સાથેની પ્રક્રિયા એ વિસ્થાપન પ્રક્રિયા છે.
પ્રવૃત્તિ 1.10 (પા.પુ. પાના નં. 11)
હેતુઃ બેરિયમ ક્લોરાઇડ અને સોડિયમ સલ્ફટ દ્વારા ઢિવિસ્થાપન પ્રક્રિયા સમજવી.
પ્રવૃત્તિઃ
- એક કસનળીમાં આશરે 3 mL બેરિયમ ક્લોરાઇડનું દ્રાવણ લો.
- બીજી કસનળીમાં આશરે 3 mL સોડિયમ સલ્ફટનું દ્રાવણ લો.
- આકૃતિ 1.9માં દર્શાવ્યા મુજબ બંને દ્રાવણોને મિશ્ર કરો.
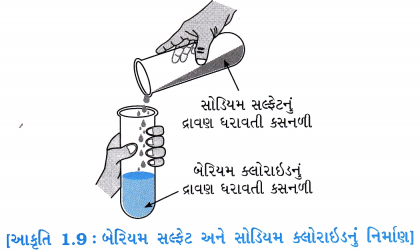
[આકૃતિ 1.9: બેરિયમ સલ્ફટ અને સોડિયમ ક્લોરાઇડનું નિર્માણ]
ઉપરોક્ત પ્રવૃત્તિ પરથી તમે શું અવલોકન કર્યું, તેના સંદર્ભમાં નીચેના પ્રશ્નોના ઉત્તર આપો :
પ્રશ્ન 1.
સોડિયમ સલ્ફટ અને બેરિયમ ક્લોરાઇડનો રંગ જણાવો.
ઉત્તર:
સોડિયમ સલ્ફટ અને બેરિયમ ક્લોરાઇડ રંગવિહીન છે.
પ્રશ્ન 2.
સોડિયમ સલ્ફટ અને બેરિયમ ક્લોરાઇડને ભેગા કરતાં શેના અવક્ષેપ મળે છે? અવક્ષેપનો રંગ જણાવો.
ઉત્તર:
સોડિયમ સલ્ફટ અને બેરિયમ ક્લોરાઇડને ભેગા કરતાં BaSO4 – બેરિયમ સલ્ફટના અવક્ષેપ મળે છે, જે સફેદ રંગના છે.
પ્રશ્ન ૩.
બેરિયમ ક્લોરાઇડ અને સોડિયમ સલ્ફટ વચ્ચે થતી ? સમતોલિત પ્રક્રિયા લખો.
ઉત્તર:
BaCl2(aq) + Na2SO4(aq) → BaSO4(s) + 2NaCl(aq)
પ્રશ્ન 4.
બેરિયમ ક્લોરાઇડ અને સોડિયમ સલ્ફટ વચ્ચે થતી પ્રક્રિયા કયા પ્રકારની છે?
ઉત્તર:
બેરિયમ ક્લોરાઇડ અને સોડિયમ સલ્ફટ વચ્ચે થતી પ્રક્રિયા એ દ્વિવિસ્થાપન પ્રકારની છે.
પ્રવૃત્તિ 1.11 (પા.પુ. પાના નં. 12)
હેતુઃ કૉપર(તાંબા)નું કૉપર ઑક્સાઇડમાં થતું ઑક્સિડેશન સમજવું.
પ્રવૃત્તિઃ
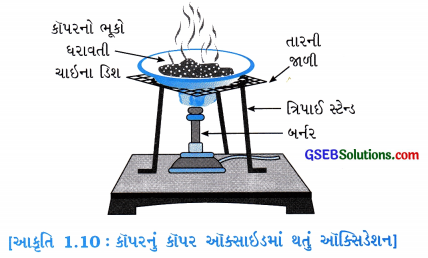
આકૃતિ 1.10માં દર્શાવ્યા મુજબ ચાઇના ડિશ(બાષ્પવાટકી)માં આશરે 1 g કૉપરનો ભૂકો લઈ, તેને ગરમ કરો.
ઉપરોક્ત પ્રવૃત્તિ પરથી તમે શું અવલોકન કર્યું, તેના સંદર્ભમાં નીચેના પ્રશ્નોના ઉત્તર આપો :
પ્રશ્ન 1.
કૉપરના ભૂકાને ગરમ કરતાં શું બને છે?
ઉત્તર:
કૉપરના ભૂકાને ગરમ કરતાં તેની સપાટી પર કૉપર (II), ઑક્સાઇડ બને છે.
પ્રશ્ન 2.
કૉપર ઑક્સાઇડનો રંગ કેવો હોય છે?
ઉત્તર:
કૉપર ઑક્સાઈડનો રંગ કાળો હોય છે.
પ્રશ્ન ૩.
કૉપરમાંથી કૉપર ઑક્સાઈડ બનવાની પ્રક્રિયા એ કયા પ્રકારની પ્રક્રિયા છે?
ઉત્તર:
કૉપરમાંથી કૉપર ઑક્સાઇડ બનવાની પ્રક્રિયા એ ઑક્સિડેશન પ્રક્રિયા છે.
2Cu + O2 ![]() 2CuO
2CuO
પ્રશ્ન 4.
ગરમ કૉપર ઑક્સાઇડ પર હાઇડ્રોજન વાયુ પસાર કરતાં કઈ નીપજ મળે છે?
ઉત્તર:
ગરમ કૉપર ઑક્સાઈડ પર હાઇડ્રોજન વાયુ પસાર કરતાં કૉપર મળે છે. જેમ કે,
CuO(s) + H2(g) ![]() Cu(s) + H2O(g)
Cu(s) + H2O(g)
![]()
પ્રશ્ન 5.
કૉપર ઑક્સાઇડમાંથી Cu મેળવવાની પ્રક્રિયા એ કયા પ્રકારની પ્રક્રિયા છે?
ઉત્તર:
કૉપર ઑક્સાઇડમાંથી Cu મેળવવાની પ્રક્રિયા એ રિડક્શન પ્રક્રિયા છે.